药用辅料行业研究丨药品一致性评价下的市场机遇

药用辅料行业研究——药品一致性评价下的市场机遇

一
1
药用辅料
市场概况
药用辅料是指在制剂处方设计时,为解决制剂的成型性、有效性、稳定性、安全性加入处方中除主药以外的一切药用物料的统称。药物辅料对药品的安全性和有效性有着直接影响,主要有赋型、调整药物功效、促进药物吸收等作用。

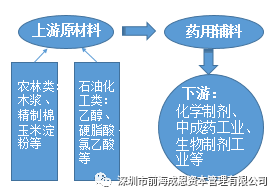
我国药用辅料行业起步于20世纪80年代,目前尚处于成长期。在我国医药行业发展中一直有“重原料,轻辅料”的倾向,虽然在2012年“毒胶囊”事件后有所改善,但我国药用辅料行业仍呈现“散、小、差”的业态。
第一,我国药用辅料行业在数量上与欧美国家还存在较大的差距。我国正在使用的药用辅料数量为550余种,而欧洲正在使用的药品辅料数量已经达到了3000种,美国也已经到了1500种。
第二,我国药用辅料行业质量较欧美地区也有较大差距,行业产能主要集中在中低端领域,国内制药企业所需的高端药用辅料需要通过进口方式向国外辅料企业以昂贵的价格采购使用。
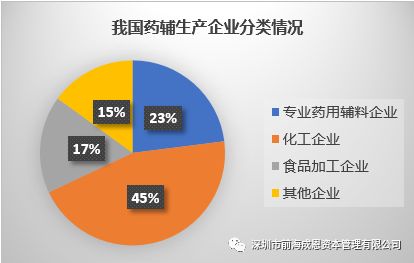
第三,我国药用辅料行业企业普遍规模偏小,市场集中度低,行业格局混乱。目前我国现有内资的药用辅料生产企业约 400 家,其中专业从事药用辅料生产的大型企业有:山河药辅、红日制药(2015 年收购湖州展望药业)、黄山胶囊、尔康制药等,市场占比约23%,总体竞争激烈,行业格局混乱。
第四,中国药用辅料行业制度体系和标准体系不完善,行业发展规范化程度低。
二
药品一致性评价与关联审评带来的机遇
目前我国药用辅料在整个药物制剂行业产值占比仅2-3%,市场规模不到400亿元,若达到发达国家5-10%的占比,将释放出300-1000亿元的市场。在国家政策以及新型制剂技术不断推广发展的情况下,我国药用辅料行业的发展机遇渐显。
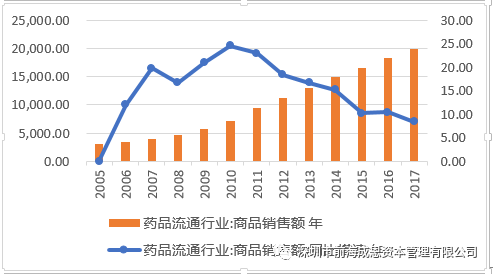
1、仿制药一致性评价政策将推动我国药用辅料行业发展。
一致性评价过程中,药用辅料对药品的药学研究和BE(一致性评价关键标准)研究均有重要影响,药学研究的主要内容就是制备工艺,辅料是制备时的重要一环,且体外溶出作为药学研究的重要评价更是与药用辅料的质量和规格密切相关;在BE实验中,药用辅料将对药品在体内的代谢吸收产生一部分的影响。
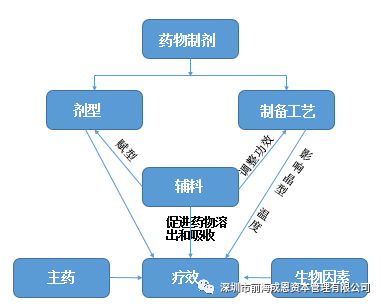
(1)一致性评价下国内药辅企业具有价格及时间的成本优势。虽然进口辅料具备技术优势,但同一种进口辅料的价格大约是国产产品的2-3倍,其引进至少需要三个月,对比之下国内药企选择国内药辅企业合作更具效率。
(2)药用辅料企业角色转型,有助于产业结构转型。基于一致性的高要求,药企在进行药品研究及生存过程中需要药用辅料企业提供持续稳定的技术和信息支持,药用辅料企业从单纯的供应商转变为合作伙伴,为药企提供定制化服务。
(3)优化药用辅料市场分配,提升行业集中度,龙头企业将收益。一致性评价严格限制药辅品种在技术工艺上的申请门槛,技术壁垒升级,技术工艺和质量竞争将成为药辅行业的竞争核心,大批中小型制药企业将面临危机,而具有先发优势并注重研发的规范化大型企业将会获益。(如山河药辅、红日制药、尔康制药等)
2、关联审评的推行将促进我国药用辅料行业规范化发展。
2016年 8 月 10 日,CFDA 发布《关于药包材药用辅料与药品关联审评审批有关事项的公告》称,自公告发布起,将直接接触药品的包装材料和容器、药用辅料由单独审批改为在审批药品注册申请时一并审评审批,标志着辅料管理从批文时代进入文档管理时代。
关联审评的推行,有利于我国药辅行业市场规模迅速扩大,优质规范药辅企业的核心竞争力将进一步突出,高标准也将为国内药用辅料企业向国际市场进发提供有力支撑。
三
重点关注方向
如前文所述,药用辅料行业正处于历史发展的机遇时期,尤其是仿制药一致性评价对药辅行业重整及产业结构升级带来的机遇,我们认为其中具备以下三个特质的企业值得我们重点关注:
(1)具备能够与药剂企业合作并开发新型辅料的工艺技术研发能力和充分产能的承载能力;
(2)具备可以为药剂企业提供持续技术服务的高标准产品质量检验流程以及专业定制化的服务能力;
(3)具备获得欧美国家认可或引进第三方认证的基础规模和能力。






